发现靶向基因转录终止的卵巢癌治疗策略!实验室最新研究成果发表
近日,实验室狄文、庄光磊团队与中国科学院上海有机化学研究所生物与化学交叉研究中心谭立团队以及复旦大学附属中山医院臧荣余团队合作,在《科学》(Science)杂志子刊《科学进展》(Science Advances)发表了题为《Therapeutic targeting of CPSF3-dependent transcriptional termination in ovarian cancer》的研究论文。该研究发现卵巢癌依赖于调控基因转录终止的CPSF蛋白复合体,阐明了其核酸内切酶CPSF3介导pre-mRNA的有效切割从而促进肿瘤发生发展的作用机制,并开发了靶向CPSF3的特异性小分子抑制剂HQY426。

卵巢癌致死率居妇科肿瘤之首,传统手术联合化疗的临床获益已经达到平台期,迫切需要深入了解卵巢癌的生物学特性,鉴定新的分子靶标并开发新型靶向药物。既往研究表明,卵巢癌基因组具有大规模染色体拷贝数变异的特点,通过致癌基因的扩增及高表达驱动肿瘤发生发展,使其对于基因转录具有独特的依赖性。近年来我院妇产科狄文、庄光磊团队与中国科学院上海有机化学研究所生物与化学交叉研究中心的谭立课题组长期合作,在Cancer Research、Oncogene等杂志发表系列研究,针对卵巢癌中调控基因转录延伸的关键激酶CDK12/13研制了新型共价抑制剂。
在最新研究中,研究人员首先在卵巢癌细胞中利用CRISPR/Cas9系统对转录终止核心调控分子逐一排查,发现干扰CPSF蛋白复合体构成基因,包括CPSF1、CPSF2、CPSF3和WDR33,在体内外模型中一致显著抑制肿瘤生长。更有意思的是,敲除这些基因都会降低核酸内切酶CPSF3的蛋白水平,并影响切割亚复合物mCF中CPSF2-CPSF3的结合,表明CPSF3在卵巢癌中发挥核心作用。研究人员进一步通过转录组测序揭示,CPSF复合体敲除主要影响了pre-mRNA 3’端终止切割,导致多聚腺苷酸化远端位点的选择增加,内含子聚腺苷酸化减少,基因转录通读上升,基因表达下降。对差异基因特征进行分析,发现DNA损伤修复基因较大,编码序列较长,外显子及多聚腺苷酸位点较多,因而更容易受到CPSF复合体异常的影响,与此结果相一致,CPSF蛋白复合体关键基因缺失后卵巢癌细胞DNA损伤明显增加。在明确CPSF3可以作为卵巢癌干预靶标的基础上,研究人员经过大量筛选和测试,开发了基于苯并硼唑母核的CPSF3特异性抑制剂HQY426。HQY426表现出优异的体内外抗卵巢癌活性,并诱导肿瘤基因组不稳定性而与PARP抑制剂具有协同作用。
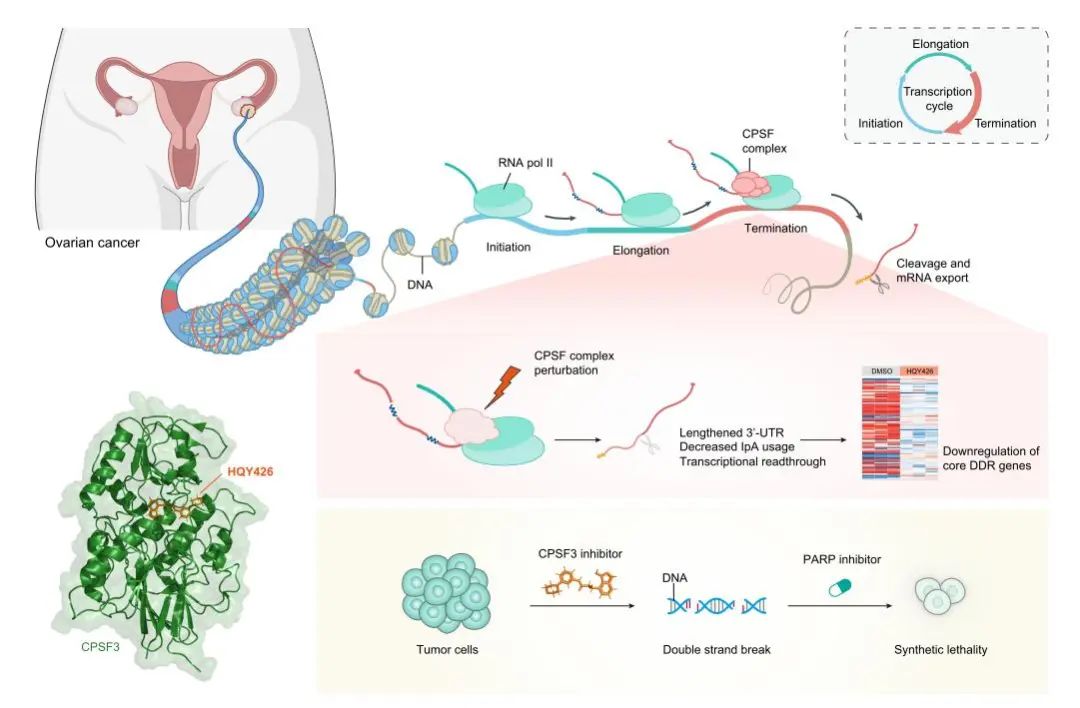
这项工作发现并证明了转录终止关键调控分子CPSF3可以作为卵巢癌的潜在治疗靶点,同时基于CPSF3开发了极具潜力的小分子化合物,为推动临床测试提供了重要理论基础和实验依据。当前,研究团队正针对CPSF3抑制剂的成药性质进行进一步优化,同时在临床前研究中拓展其应用场景。
上海市妇科肿瘤重点实验室的助理研究员沈佩烨、博士研究生叶凯雁、助理研究员张振峰与谭立课题组的博士研究生项淮江为本文共同第一作者。实验室主任狄文教授、副主任庄光磊研究员、中国科学院上海有机化学研究所生物与化学交叉研究中心的谭立研究员以及复旦大学附属中山医院臧荣余教授为本文共同通讯作者。该工作得到国家自然科学基金委、上海市科委、上海市教委和中国科学院的资助。
联系人:李青
电话:021-68382070
地址:上海市浦建路160号17号楼10楼
Copyright© 上海市妇科肿瘤重点实验室 沪ICP备09022836号  沪网安备31011502003436
沪网安备31011502003436