揭示CDK12/13双重抑制在卵巢癌治疗的两面性
实验室主任狄文教授、副主任庄光磊研究院与中科院谭立教授合作发表文章
近日,实验室主任狄文教授、庄光磊教授与中国科学院生物与化学交叉研究中心谭立课题组近日在Cancer Research期刊上发表研究论文“Dual inhibition ofCDK12/CDK13 targets both tumor and immune cells in ovarian cancer”,报道了基于亚砷酸弹头的高活性、高特异性、且具备口服生物利用度的有机胂CDK12/13抑制剂ZSQ836的研制,以及对CDK12/13作为卵巢癌治疗靶点可行性的进一步评估。

该项研究发现,利用亚砷酸共价弹头替代常用的靶向半胱氨酸的丙烯酰胺类共价弹头、基于结构导向设计研制的ZSQ836不但在活性与特异性上均与THZ531相当,且在药代动力学性质上远优于后者(图1)。
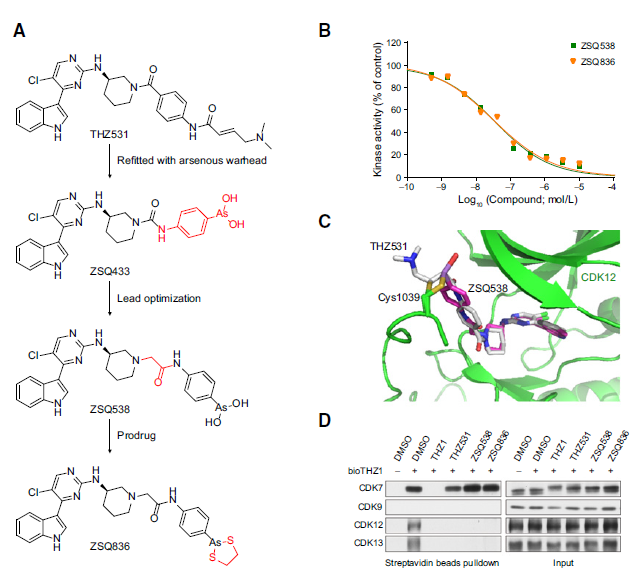
在免疫缺陷的小鼠模型上,ZSQ836很好地抑制了卵巢癌肿瘤的生长,并与铂类化疗药物或PARP抑制剂产生显著的协同疗效。然而,在免疫正常的小鼠模型上,CDK12/13的双重抑制不但在癌细胞中显著下调了多个促癌基因、并引起DNA损伤,同时还抑制了T细胞的增殖与激活,进而限制了肿瘤中的淋巴浸润(图2)。
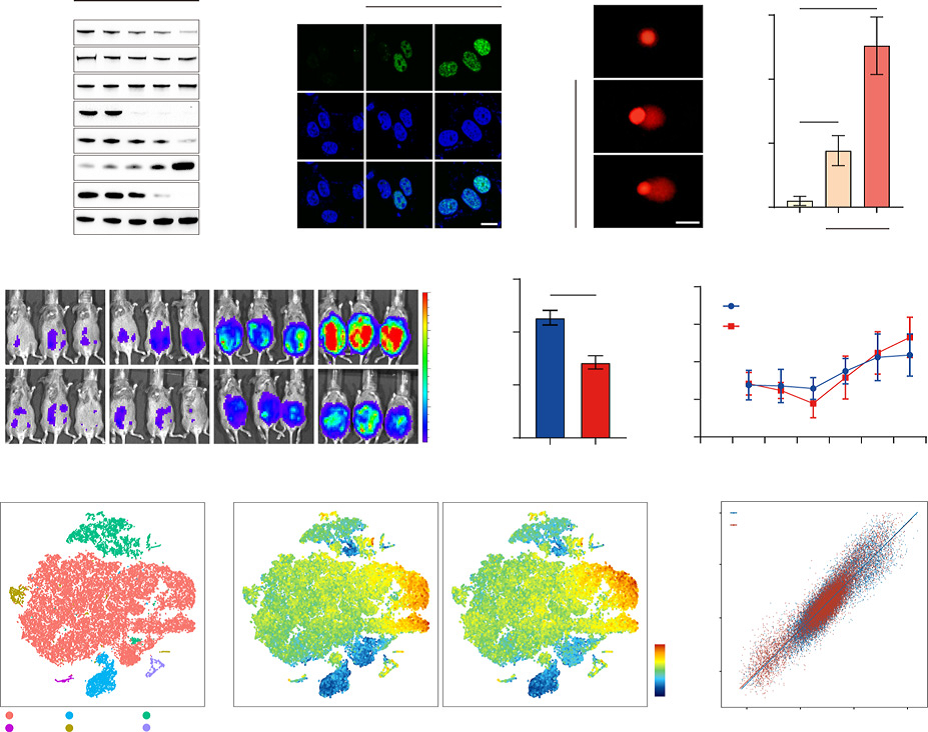
卵巢癌是妇科肿瘤中致死率最高的恶性肿瘤,探寻创新有效的治疗策略,提高患者预后是目前卵巢癌研究领域的重中之重。目前铂类化疗药物与PARP抑制剂是卵巢癌临床治疗的主要药物。细胞周期蛋白激酶CDK12及其同源的CDK13,因对超级增强子驱动的癌基因、DNA损伤修复基因的表达起重要调控作用,被认为是卵巢癌以及其他恶性肿瘤临床治疗的潜在靶标。基于丙烯酰胺类共价弹头的THZ531,通过共价靶向CDK12/13激酶域保守的半胱氨酸残基实现对其高活性、高特异性的抑制,然而却受限于药代性质难以进一步应用于动物模型研究;而SR-4835等其他非共价抑制剂,则是通过分子胶水机制降解Cyclin-K,进而间接抑制CDK12/13的激活。
联系人:李青
电话:021-68382070
地址:上海市浦建路160号17号楼10楼
Copyright© 上海市妇科肿瘤重点实验室 沪ICP备09022836号  沪网安备31011502003436
沪网安备31011502003436